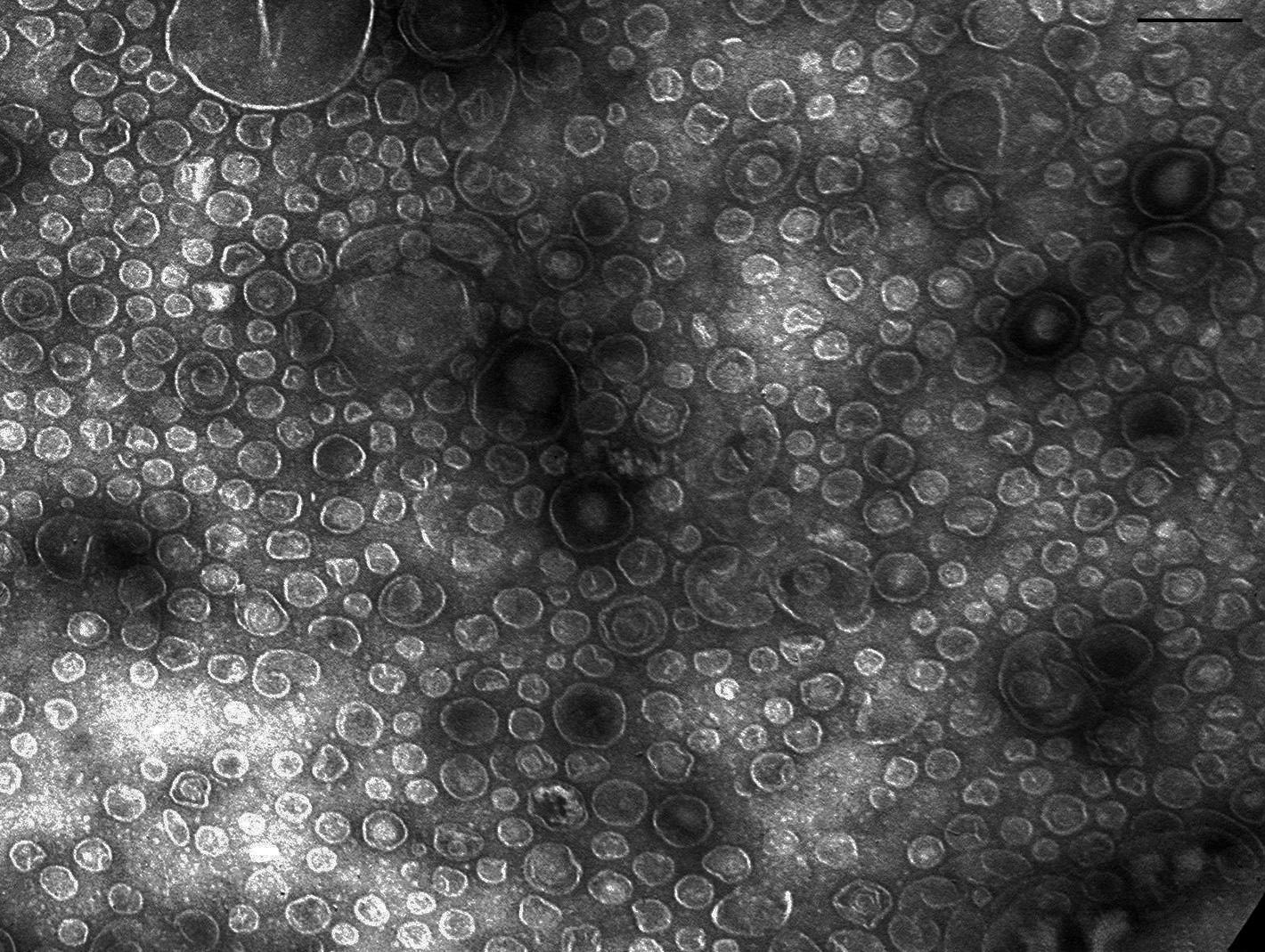
Везикулы долгое время считались клеточным мусором, однако в середине прошлого века выяснилось, что это вовсе не так. Эти наноконтейнеры, внутри которых могут содержаться различные вещества, служат своеобразной «почтой» для обмена информацией. С помощью везикул клетки влияют на то, какие процессы происходят в соседних клетках. Это вызывает особый интерес со стороны исследователей, поскольку пузырьки можно использовать в качестве транспорта для доставки лекарственных средств.
Новая публикация ученых обобщает целый цикл работ, посвященных изучению формирования везикул у Lysobacter sp. XL1. Штамм Lysobacter sp. XL1 интересен тем, что способен синтезировать комплекс бактериолитических белков, то есть разрушающих клеточные стенки других бактерий, приводя их к гибели. Такие белки можно использовать для создания антибактериальных препаратов нового поколения, альтернативных антибиотикам.
Во внешнюю среду бактериолитические белки выходят разными путями, в том числе и прячась внутри везикул, как например в случае с белком Л5, — «убийцей» клеток конкурентов Lysobacter sp. XL1. Грамотрицательные бактерии, к которым относится и Lysobacter sp. XL1, имеют две мембраны, отделенные периплазмой, — в результате выпячивания внешней мембраны происходит отпочковывание везикул, наполненных биологически активными соединениями, например бактериолитическими белками.
«Есть много моделей того, как именно формируются везикулы грамотрицательных бактерий. Согласно одной из них, они образуются из участков внешней мембраны, "жесткость" которых нарушена. Согласно другой модели, в формировании везикул принимает участие клеточный "мусор": неправильно свернутые белки, фрагменты компонентов бактериальной клеточной стенки. Мы предполагаем, что одного фактора здесь недостаточно и теория образования везикул сложнее» — рассказывает руководитель проекта по гранту РНФ Ирина Кудрякова, кандидат биологических наук, старший научный сотрудник лаборатории биохимии клеточной поверхности микроорганизмов ИБФМ РАН.
Ранее сотрудники Института биохимии и физиологии микроорганизмов имени Г. К. Скрябина РАН (Пущино)
провели исследования, которые позволили предположить, что в образовании везикул Lysobacter sp. XL1 может принимать участие Л5. Эта гипотеза возникла из-за того, что бактерия образует несколько видов везикул, и один из них содержит белок-«убийцу». Авторы установили, что он концентрируется в периплазме ближе к внешней мембране бактерии.
Оказалось, что некоторые ее участки обогащены отрицательно заряженным фосфолипидом кардиолипином, дестабилизирующим внешнюю мембрану за счет отталкивания отрицательных зарядов, — здесь и происходит образование везикул с Л5.

Коллектив лаборатории. Источник: Ирина Кудрякова
Чтобы проверить свою гипотезу, в новой работе биологи создали штамм бактерии Lysobacter sp. XL1, у которого ген этого белка выключен, то есть Л5 не производится, — это стало непростой задачей, поскольку микроорганизм недостаточно хорошо изучен и мало методик по его генетическим модификациям.
Оказалось, что без белка Л5 бактерия образовывала меньшее количество везикул. Кроме того, практически полностью утратились их литические свойства (способность разрушать бактериальные клетки). Таким образом, авторы доказали участие белка Л5 в образовании везикул Lysobacter sp. XL1.
«Успешное отключение гена белка Л5 у Lysobacter sp. XL1 открывает многие перспективы. Бактериолитический белок Л5 перспективен для создания антимикробных препаратов нового поколения, нацеленных на борьбу с штаммами, устойчивыми к многим антибиотикам, а внешнемембранные везикулы Lysobacter sp. XL1 представляют собой хорошую модель для конструирования эффективных препаратов», — рассказывает Ирина Кудрякова.
Предложенная авторами модель позволит по-новому взглянуть на этот процесс у грамотрицательных бактерий.