В результате самых разных заболеваний — например, инфаркта, инфекций легких, гепатита и других — возникает фиброз. Это разрастание соединительной ткани, которая замещает любую другую поврежденную ткань. Из-за того, что соединительная ткань не способна выполнять функции той, что была ранее на ее месте, работоспособность соответствующего органа ухудшается. По статистике, такие последствия фиброза объясняют почти 50% смертей в развитых странах.
Ключевую роль в развитии фиброза играет воспалительный процесс. С одной стороны, он полезен для организма, поскольку позволяет бороться с инфекциями, но с другой, став хроническим, он приводит к обширному фиброзу и, соответственно, повреждению органа. Хроническое воспаление обеспечивают определенные клетки иммунной системы — так называемые макрофаги М2. Однако за счет чего они вызывают такой эффект, остается не до конца понятным, а потому остановить развитие фиброза пока практически невозможно.
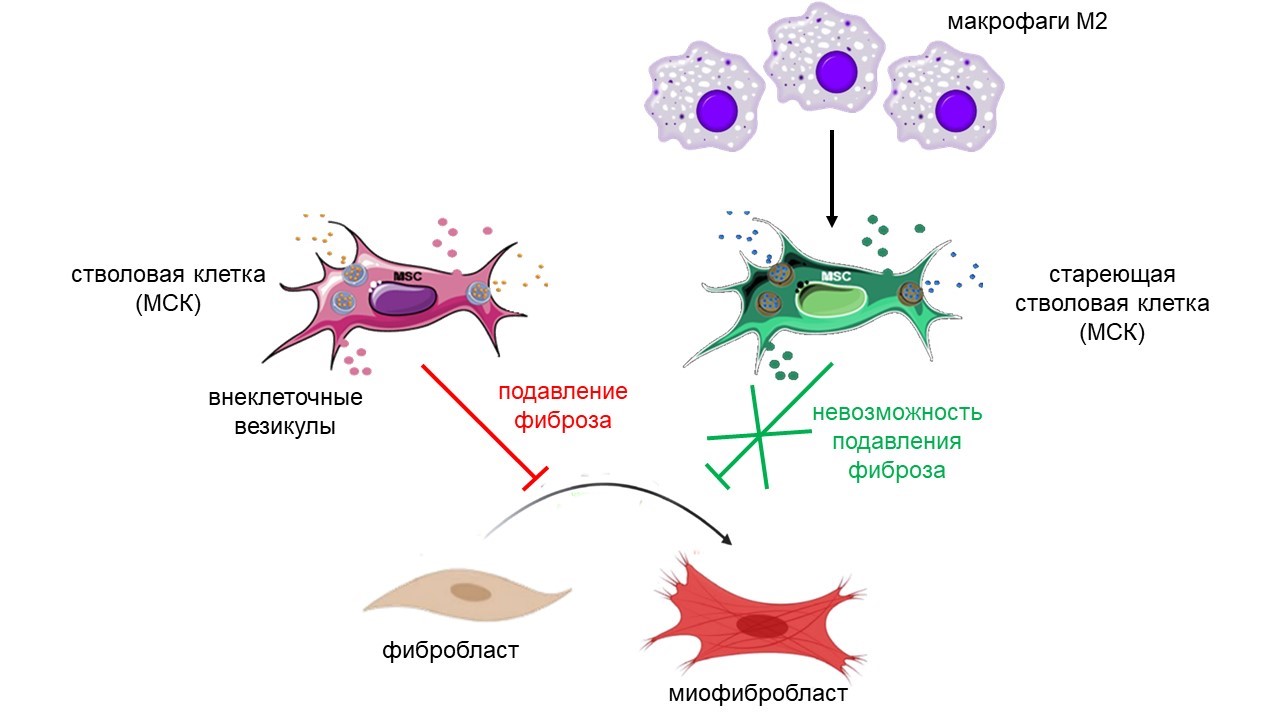
Схема взаимодействия макрофагов, стволовых клеток и фибробластов. Источник: Ольга Григорьева.
Ученые из Московского государственного университета имени М. В. Ломоносова (Москва) исследовали роль макрофагов М2 в развитии фиброза. За правильное восстановление тканей (без фиброза) отвечают стволовые клетки. Они подавляют превращение нормальных клеток ткани в миофибробласты — тип клеток, отвечающих за возникновение и прогрессирование фиброза. Это значит, что при нормальной работе стволовых клеток заболевание не возникает. Чтобы проверить, как на стволовые клетки влияют макрофаги М2, авторы выдерживали стволовые клетки вместе с белками, полученными от макрофагов, на чашках Петри в течение 48 часов. Эксперимент показал, что добавление таких соединений приводит к старению стволовых клеток, в результате чего они теряют способность подавлять образование миофибробластов и больше не могут обеспечивать восстановление нормальных тканей.
На старение стволовых клеток в присутствии макрофагов М2 указало то, что в них увеличилось количество белка р21, тормозящего деление. Кроме того, в этом случае стволовые клетки выделяли до шести раз больше провоспалительных молекул и других веществ, способствующих развитию фиброза, чем в обычных (контрольных) условиях.
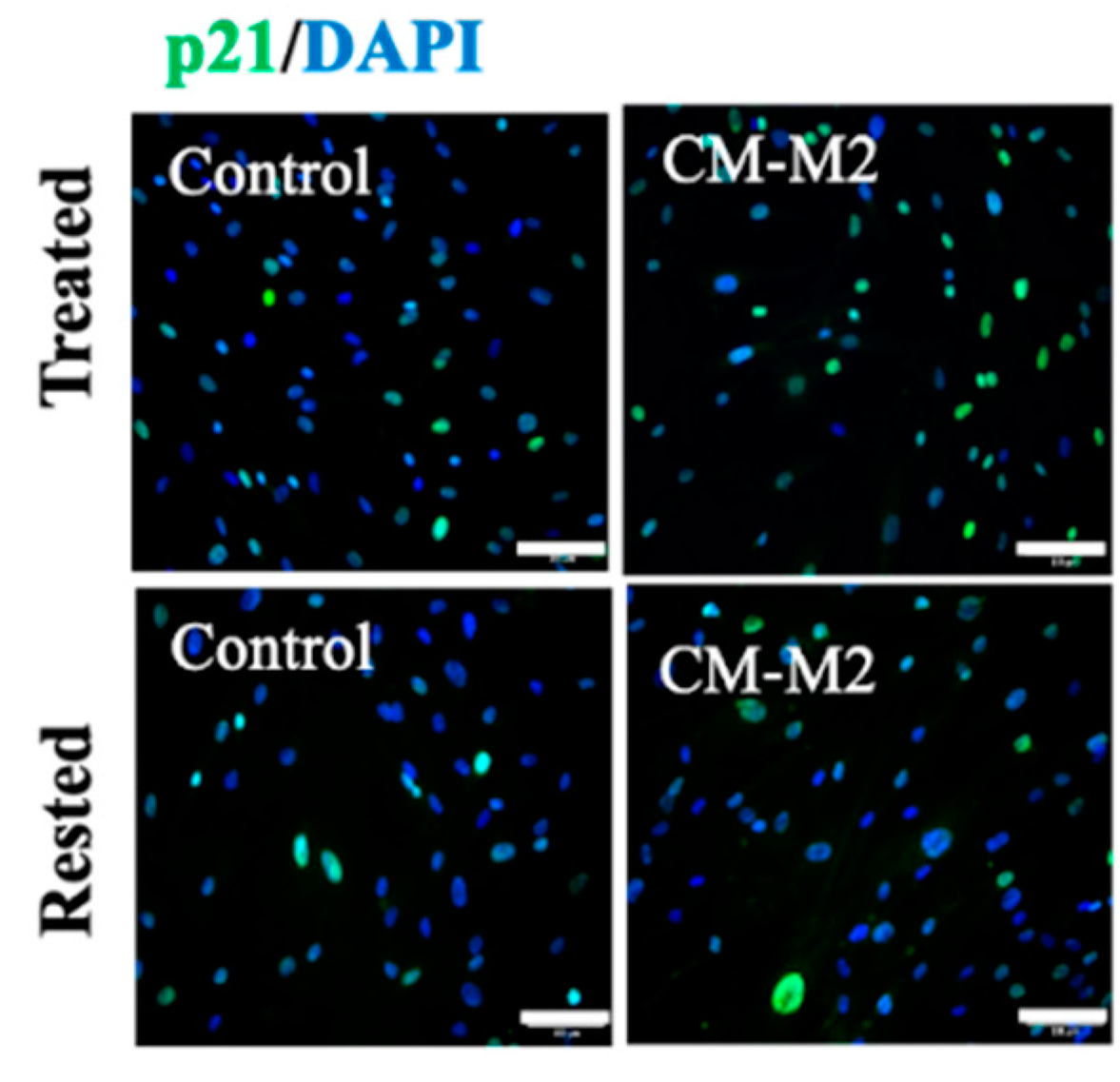
Активность гена р21 — маркера старения — в контрольных стволовых клетках и культурах, 48 часов испытывавших влияние макрофагов М2. Источник: Dyachkova et al. / International Journal of Molecular Sciences, 2023.
Авторы также провели эксперимент, который позволил подтвердить, что стареющие стволовые клетки не способны подавлять развитие фиброза. Для этого исследователи обработали фибробласты — клетки соединительной ткани человека — микровезикулами — пузырьками с ферментами и другими биологически активными соединениями, которые выделяют в окружающую среду как обычные стволовые клетки, так и те, что 48 часов находились вместе с белками макрофагов М2. Оказалось, что в первом случае развитие миофибробластов подавлялось, тогда как во втором никакого влияния на уменьшение фиброза не было. Это указывает на то, что для эффективного предотвращения фиброза нужно, чтобы стволовые клетки не испытывали влияния макрофагов М2.
«Эксперименты показали, что макрофаги М2 вызывают старение стволовых клеток, из-за чего те теряют способность бороться с фиброзом. Это открытие можно использовать при разработке препаратов для профилактики фиброза, например, создавая соединения, которые будут избирательно подавлять активность макрофагов М2 и тем самым оберегать стволовые клетки от их воздействия. В дальнейшем мы планируем разработать системы для целевого удаления М2-макрофагов из тканей модельных животных и изучить в этой системе вклад макрофагов в развитие фиброза на уровне организма. Кроме того, мы хотим провести доклинические испытания микровезикул как потенциального средства для борьбы с фиброзом», — рассказывает участник проекта, поддержанного грантом РНФ, Ольга Григорьева, кандидат биологических наук, старший научный сотрудник института регенеративной медицины МГУ имени М. В. Ломоносова.Если вы хотите стать героем публикации и рассказать о своем исследовании, заполните форму на сайте РНФ