Во всех живых клетках гены работают с разной интенсивностью: одни очень активны и обеспечивают продукцию большого количества нужного организму белка, а другие могут долгое время «молчать». Своевременное и точное включение нужных генов и поддержание их активности позволяет организму правильно развиваться и функционировать. При этом, управляя их активностью, можно изучать механизмы развития генетических заболеваний. Кроме того, контроль за работой генов позволит увеличить точность систем редактирования генома и эффективность ряда генотерапевтических препаратов. Однако существующие на сегодняшний день системы направленной активации нужных генов несовершенны: их трудно доставлять в клетки из-за большого размера, а также они не всегда специфичны, то есть активируют помимо гена-мишени еще несколько других.
Ученые из Московского государственного университета имени М. В. Ломоносова (Москва) предложили новую компактную молекулярную систему, способную работать как искусственный белок-транскрипционный фактор и активировать только нужные гены. За основу ученые взяли вирусный фермент Cre-рекомбиназу, которая в норме разрезает молекулу ДНК строго в определенном месте, таким образом участвуя в процессе размножения вируса. При этом фермент находит место, в которое нужно внести разрыв, по последовательности букв-нуклеотидов в ДНК. Обнаружив этот «пароль», рекомбиназа связывается с молекулой ДНК.
.jpg)
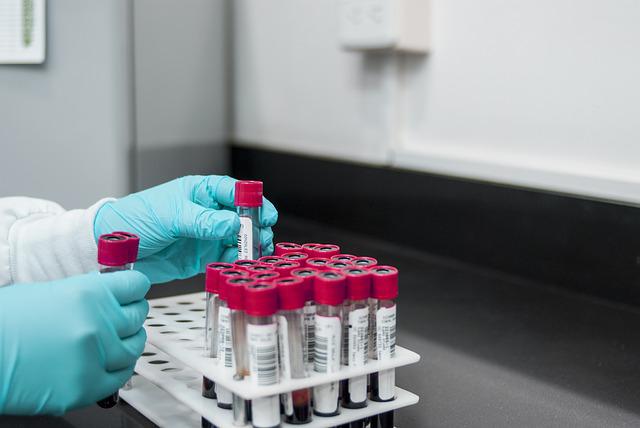
Флуоресценция опухолевых клеток почечного эпителия человека до активации гена зеленого флуоресцентного белка и после. Источник: Karagyaur et al. / Cells, 2022.
В данной работе авторы использовали неактивную Cre-рекомбиназу, которая была неспособна разрезать ДНК, но при этом точно находила нужный для ее посадки сайт и связывалась с ним. К рекомбиназе биологи присоединили фрагмент транскрипционного фактора, задача которого состояла в активации генов. В результате рекомбиназа доставляла активатор строго в нужные участки ДНК, а именно на искусственные промоторы — посадочные места для регуляторных белков. Специфичность рекомбиназы обеспечила высокую точность и всей предложенной системы.
Ученые проверили предложенный метод на опухолевых клетках почечного эпителия человека, активировав с его помощью искусственно внесенный ген зеленого флуоресцентного белка, а также несколько других генов, в том числе кодирующий фактор роста, а также систему редактирования генома CRISPR/Cas9. Последний ген был выбран для того, чтобы проверить, можно ли использовать предложенную систему в генной терапии как способ повышения эффективности и специфичности CRISPR/Cas9.
Через двое суток светимость опухолевых клеток увеличилась до двадцати раз, и это доказало, что ген флуоресцентного белка успешно активировался. Кроме того, авторы подтвердили, что количество РНК, считанной с остальных исследованных последовательностей, возросло до 800 раз. Это подтвердило, что данная разработка может использоваться для активации самых разных генов при решении задач генной терапии, регенеративной медицины, биотехнологического производства и фундаментальных исследований.
«Предложенная нами система позволяет контролировать нужный ген и при необходимости в сотни раз увеличивать его активность, не влияя при этом на работу остальных последовательностей ДНК в клетке. Это поможет повысить эффективность методов редактирования генома, а также может использоваться в генной терапии и биотехнологическом производстве. В дальнейшем мы планируем усовершенствовать свою разработку, чтобы сделать ее более удобной для широкомасштабного применения», — рассказывает Максим Карагяур, кандидат биологических наук, старший научный сотрудник Института регенеративной медицины МНОЦ МГУ.
Если вы хотите стать героем публикации и рассказать о своем исследовании, заполните форму на сайте РНФ.







.jpg)

