






Семейная гиперхолестеринемия — это наследственное заболевание, при котором генетическое повреждение является причиной высокого уровня холестерина крови, что, в свою очередь, проявляется в развитии атеросклероза и сердечно-сосудистых заболеваний. В 85—90 % это заболевание связано с нарушениями в работе гена рецепторов ЛПНП, которые в гетерозиготной форме присутствуют приблизительно у одного из трехсот человек. Таким образом, речь идет об очень большом количестве людей, оказывающихся в группе риска развития этой наследственной патологии.
Ее изучением на протяжении ряда лет в рамках проектов, поддержанных грантами Российского научного фонда, занимаются сотрудники лаборатории эпигенетики развития совместно с коллегами из НИИ медгенетики Томского национального исследовательского медицинского центра РАН и Московского национального исследовательского медицинского центра кардиологии имени академика Е. И. Чазова Министерства здравоохранения Российской Федерации. Как и в случае с рядом других заболеваний, исследования проводят с помощью клеточных моделей, полученных из индуцированных плюрипотентных стволовых клеток реальных пациентов, что открывает перед учеными новые возможности.
Ранее было известно, что нарушения в гене рецепторов ЛПНП сказываются на работе клеток печени — гепатоцитов, которые перестают улавливать холестерин в нужных объемах, он копится в кровеносной системе. Это приводит к образованию атеросклеротических бляшек, а те в свою очередь вызывают повреждения внутреннего слоя кровеносных сосудов, состоящего из эндотелиальных клеток.
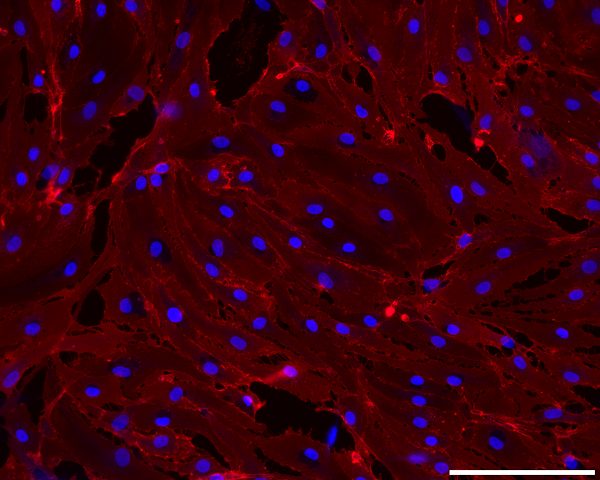
«Мы стали первыми, кто изучал влияние нарушений гена рецепторов ЛПНП на сами эндотелиальные клетки. С помощью клеточной модели пациента мы смогли узнать, что происходит с этими клетками, даже если они не вступали в контакт с атеросклеротической бляшкой, сравнили их с аналогичными клетками здоровых людей. И доказали, что нарушения в работе гена рецепторов ЛПНП сами по себе негативно влияют на клетки сосудов», – рассказала старший научный сотрудник ФИЦ ИЦиГ СО РАН кандидат биологических наук Ирина Сергеевна Захарова.
Результаты исследований, проведенных на клеточных моделях, помимо расширения знаний о механизмах развития распространенного наследственного заболевания, имеют и очевидное прикладное значение.
Во-первых, они подтверждают преимущества, которые дают такие клеточные модели в подборе эффективных средств терапии для лечения СГХС. Это актуальная проблема, поскольку не более 3—6 % пациентов с гетерозиготной формой заболевания в результате лечения показывают восстановление до нормальных показателей холестерина. Улучшить статистику можно с помощью подбора лекарств с учетом класса нарушений в гене (сегодня их выделено пять), а в идеале — индивидуальных особенностей пациента. Как минимум, выбирая новые цели для терапии, необходимо учитывать выявленное влияние нарушений на сами клетки сосудов, но встает вопрос, как осуществить этот подбор.
«Животные, в силу различий в метаболизме, плохо подходят для испытаний лекарственных препаратов. Есть свои недостатки и у клеточных моделей, где нарушения в работе гена были созданы искусственно. Наши модели, созданные из клеток реальных пациентов, дают более релевантные результаты, являясь действенным инструментом развития персонифицированной медицины», — объяснила Ирина Захарова.
Во-вторых, проводя дальнейшие исследования эндотелиальных клеток больных СГХС, ученые ИЦиГ показали, что с помощью CRISPR/Cas-опосредованных методов их можно отредактировать и восстановить функциональность клеток до нормы.
Работы по клиническому применению геномного редактирования для лечения пациентов с СГХС уже ведутся за рубежом. В конце прошлого года было объявлено о начале кинических испытаний препарата, исправляющего нарушения в другом гене пациента. Правда, в отличие от гена рецепторов ЛПНП, он отвечает только за 1—2 % случаев заболевания. Тем не менее, по оценке Ирины Захаровой, объединение опыта создания подобных препаратов с имеющимися результатами исследований ученых из ФИЦ ИЦиГ СО РАН откроет хорошие перспективы для дальнейшего развития терапии атеросклероза.

