






Наши клетки имеют множество механизмов защиты от всевозможных повреждений, как внешних, так и внутренних. Среди молекул-«защитников» особое внимание ученых на протяжении последних тридцати лет привлекает маленький, но очень важный белок p53. Его главная задача – защита генетического материала. Пока все хорошо, активность крошечного «хранителя» сдерживается в результате взаимодействия с другим белком, MDM2. В его присутствии p53 разрушается, однако, из-за постоянного синтеза новых молекул «хранителей» клетка не остается без защиты.
При повреждении или угрозе повреждения ДНК маленький «хранитель» активирует синтез белков-«спасателей», запуская целый каскад ответных реакций – репарационных (ремонтных) команд. В результате клетка словно замирает – останавливается клеточный цикл и удвоение ДНК – до тех пор, пока дефект не будет устранен. Если опасность миновала или повреждение не очень серьезное, то рано или поздно жизнь клетки станет прежней. Однако порой репарационные команды белков неспособны справиться с восстановлением нормальной структуры ДНК, и ничего не остается, кроме как убить дефектную клетку, нанеся минимальный вред организму. В любом случае поврежденный наследственный материал не сохранится в следующих поколениях и, соответственно, не вызовет развитие опухоли.
Впрочем, пессимистичный вариант тоже есть. При различных мутациях наблюдается повышенная экспрессия (синтез) белка MDM2, и он начинает показывать свою онкогенную – способствующую развитию опухоли – сущность. Связанный им p53 больше не способен работать даже в критической для клетки ситуации. Поскольку никаких SOS-сигналов нет, поврежденный генетический материал накапливается и передается следующему клеточному поколению, что приводит к развитию рака. В некоторой степени можно предотвратить такие события, если блокировать связывание MDM2 с «хранителем генома» p53 – на этом и основано действие новых разработанных препаратов.
«Мы провели цикл исследований, посвященных созданию ингибиторов, подавителей, белок-белкового взаимодействия MDM2-p53. Подобная работа возможна благодаря сочетанию в рамках одной лаборатории трех основных компонентов медицинской химии: высокопроизводительных расчетов, химического синтеза и исследования целевой биологической активности полученных нами соединений», – рассказывает Александр Гарабаджиу, известный специалист в области химии и технологии биологически активных веществ, доктор химических наук, профессор, проректор по научной работе СПбГТИ (ТУ).
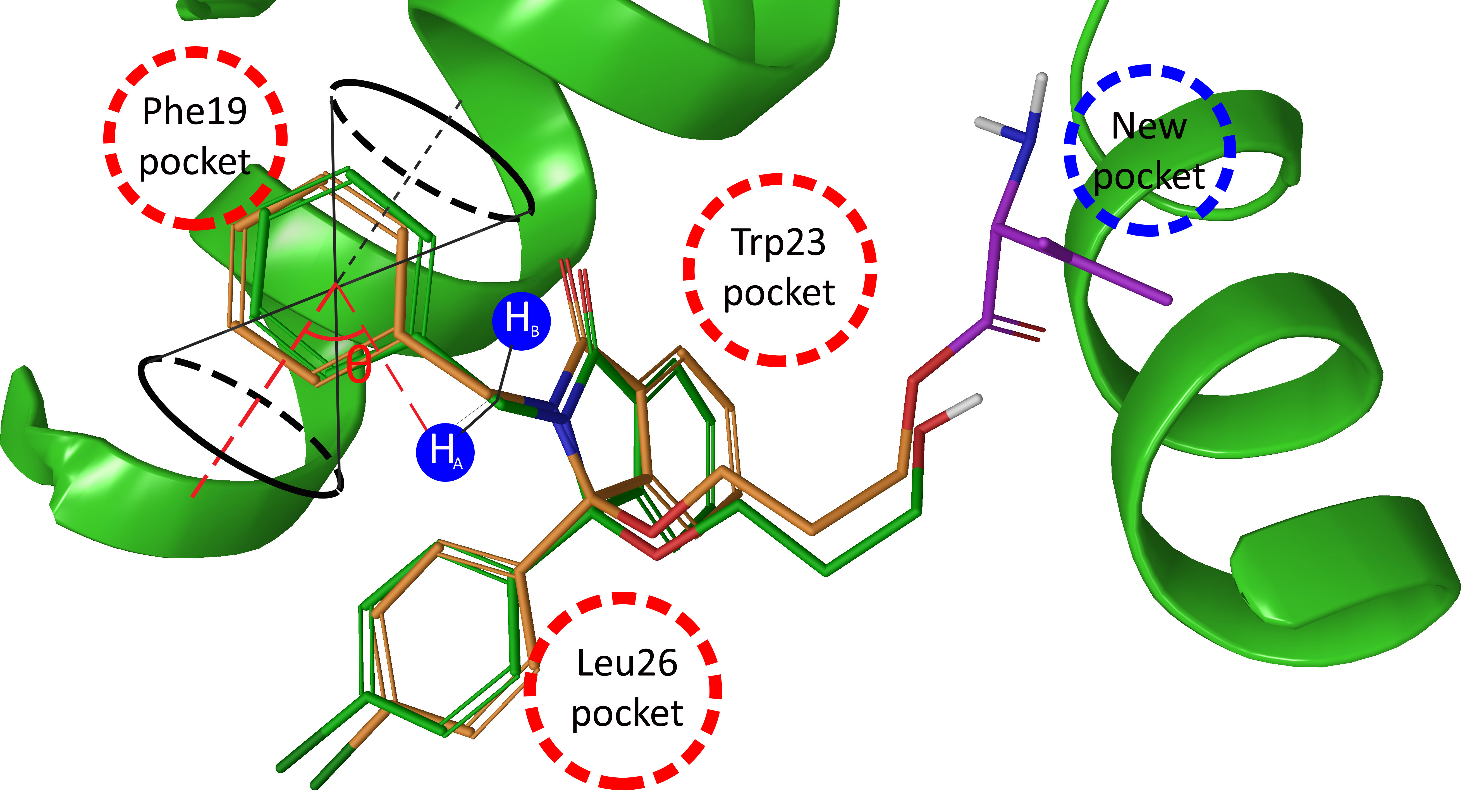
На основе глубокого изучения структуры белка MDM2 и компьютерного моделирования его взаимодействия с p53 ученые выдвинули новую гипотезу. Они предложили создать в малой молекуле ингибитора – вещества, замедляющего реакцию – дополнительный центр связывания с белком MDM2. Эффективность такого подхода подтвердилась в ходе испытаний in vitro на белковых и клеточных моделях: полученные соединения успешно блокируют MDM2, из-за чего повышается активность белка p53. Использование новых методов способно как повысить действенность уже известных лекарств-активаторов за счет модификации их структуры, так и привести к разработке новых соединений.
«В настоящий момент завершены эксперименты с новым классом активаторов р53. Созданные нами соединения обладают активностью, превышающей наиболее мощные препараты, развиваемые в передовых научных центах США и Европы. Лекарства, основанные на активации р53, способны стать новым шагом на пути к созданию эффективных и безопасных средств для химиотерапии раковых заболеваний», — заключает Александр Гарабаджиу.

